Uploaded on authorSTREAM by SUSMININGSIH
ISOMER, ppt
Ditulis dalam MATERI KIMIA
ISOMER
Dalam ilmu kimia, isomer ialah molekul-molekul dengan rumus kimia yang sama (dan sering dengan jenis ikatan yang sama), namun memiliki susunan atom yang berbeda (dapat diibaratkan sebagai sebuah anagram). Kebanyakan isomer memiliki sifat kimia yang mirip satu sama lain. Juga terdapat istilah isomer nuklir, yaitu inti-inti atom yang memiliki tingkat eksitasi yang berbeda.
Contoh sederhana dari suatu isomer adalah C3H8O. Terdapat 3 isomer dengan rumus kimia tersebut, yaitu 2 molekul alkohol dan sebuah molekul eter. Dua molekul alkohol yaitu 1-propanol (n-propil alkohol, I), dan 2-propanol (isopropil alkohol, II). Pada molekul I, atom oksigen terikat pada karbon ujung, sedangkan pada molekul II atom oksigen terikat pada karbon kedua (tengah). Kedua alkohol tersebut memiliki sifat kimia yang mirip. Sedangkan isomer ketiga, metil etil eter, memiliki perbedaan sifat yang signifikan terhadap dua molekul sebelumnya. Senyawa ini bukan sebuah alkohol, tetapi sebuah eter, dimana atom oksigen terikat pada dua atom karbon, bukan satu karbon dan satu hidrogen seperti halnya alkohol. Eter tidak memiliki gugus hidroksil.
Isomer
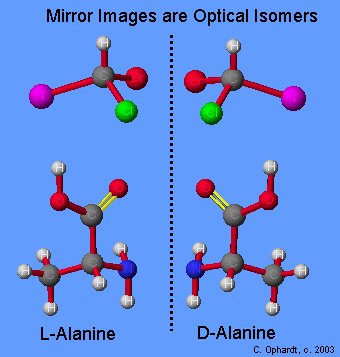
Terdapat dua jenis isomer, yaitu isomer struktural dan stereoisomer. Isomer struktural adalah isomer yang berbeda dari susunan/urutan atom-atom terikat satu sama lain. Contoh yang disebutkan diatas termasuk kedalam isomer struktural. Sedangkan stereoisomer memiliki struktur yang sama, namun beberapa atom atau gugus fungsional memiliki posisi geometri yang berbeda.
Ditulis dalam MATERI KIMIA
TATA NAMA SENYAWA KARBON,ppt
Ditulis dalam MATERI KIMIA
MY MUSIC COLLECTION
Ditulis dalam Music
LATIHAN SOAL KIMIA
Kami menyediakan latihan soal kimia yang bermanfaat dalam membantu para siswa untuk belajar memahami materi kimia. Silahkan klik Latihan Kimia 1, untuk mendapatkan contoh soal-soal kimia
Ditulis dalam SOAL KIMIA
COVALENT BOND
How do you know if it is a covalent bond? A covalent bond is formed when electrons are shared between atoms. Covalent bonds are between non-metals and non-metals or hydrogen and non-metals. They share electrons so that both of them can have a stable octet.
Ditulis dalam MATERI KIMIA
OXIDATION-REDUCTION
OXIDATION-REDUCTION
An important concept of chemical reactions which is useful in systematizing the chemistry of many substances. Oxidation can be represented as involving a loss of electrons by one molecule and reduction as involving an absorption of electrons by another. Both oxidation and reduction occur simultaneously and in equivalent amounts during any reaction involving either process.
REACTIONS
In an oxidation-reduction reaction, some element decreases in oxidation state and some element increases in oxidation state. The substances containing these elements are defined as the oxidizing agents and reducing agents, and they are said to be reduced and oxidized, respectively. The processes in question can always be represented formally as involving electron absorption by the oxidizing agent and electron donation by the reducing agent..
VIDEO :
Ditulis dalam MATERI KIMIA
ELEKTROLIT
ELEKTROLIT
Elektrolit adalah suatu zat yang larut atau terurai ke dalam bentuk ion-ion dan selanjutnya larutan menjadi konduktor elektrik, ion-ion merupakan atom-atom bermuatan elektrik. Elektrolit bisa berupa air, asam, basa atau berupa senyawa kimia lainnya. Elektrolit umumnya berbentuk asam, basa atau garam. Beberapa gas tertentu dapat berfungsi sebagai elektrolit pada kondisi tertentu misalnya pada suhu tinggi atau tekanan rendah. Elektrolit kuat identik dengan asam, basa, dan garam kuat. Elektrolit merupakan senyawa yang berikatan ion dan kovalen polar. Sebagian besar senyawa yang berikatan ion merupakan elektrolit sebagai contoh ikatan ion NaCl yang merupakan salah satu jenis garam yakni garam dapur. NaCl dapat menjadi elektrolit dalm bentuk larutan dan lelehan. atau bentuk liquid dan aqueous. sedangkan dalam bentuk solid atau padatan senyawa ion tidak dapat berfungsi sebagai elektrolit.
VIDEO EKSPERIMEN:
Ditulis dalam MATERI KIMIA
HISTORY OF THE ATOM
HISTORY OF THE ATOM
By : Dra. SUSMININGSIH
Democritus develops the idea of atoms (460 BC)
He pounded up materials in his pestle and mortar until he had reduced them to smaller and smaller particles which he called Atoma ((greek for indivisible).
John Dalton (1808)
Suggested that all matter was made up of tiny spheres that were able to bounce around with perfect elasticity and called them atoms.
Joseph John Thompson (1898)
Found that atoms could sometimes eject a far smaller negative particle which he called an electron.
Ernest Rutherford (1910)
Oversaw Geiger and Marsden carrying out his famous experiment. They fired Helium nuclei at a piece of gold foil which was only a few atoms thick. They found that although most of them passed through. About 1 in 10,000 hit.
Niels Bohr (1913)
Studied under Rutherford at the Victoria University in Manchester. Bohr refined Rutherford’s idea by adding that the electrons were in orbits. Rather like planets orbiting the sun. With each orbit only able to contain a set number of electrons.
VIDEO :
Ditulis dalam MATERI KIMIA
What is an atom?
ATOM
Atom is the smallest particle of an element which cannot be devided further. Atom is the smallest particle of an element that still has the same character with or as in original elements.
PARTICLES THAT FORM ATOM
An atom consists of 3 kinds of base particles namely proton and neutron are in the nucleus of the atom, whereas the other particle, electron, is moving in the space around the nucleus.
VIDEO:
Ditulis dalam MATERI KIMIA


Komentar Terbaru